 服務(wù)熱線:400-8822-003
服務(wù)熱線:400-8822-003
 服務(wù)熱線:400-8822-003
服務(wù)熱線:400-8822-003
 更新時(shí)間:2026-02-06
更新時(shí)間:2026-02-06 點(diǎn)擊次數(shù):132
點(diǎn)擊次數(shù):132
引言
在腫瘤的微環(huán)境里,每一類細(xì)胞都攜帶著自己獨(dú)特的代謝庫。
上周,一位創(chuàng)新藥企的研發(fā)總監(jiān)向我們提出了一個(gè)尖銳而典型的問題:“我們?cè)O(shè)計(jì)的前藥,在肝微粒體里活化數(shù)據(jù)很好,但一到細(xì)胞實(shí)驗(yàn)里效果就不穩(wěn)定……問題到底出在哪里?"
這個(gè)疑問,像一把鑰匙,打開了臨床前藥物代謝研究中的一個(gè)關(guān)鍵盲區(qū):我們是否過于依賴“標(biāo)準(zhǔn)答案"——肝微粒體模型,而忽視了藥物最終的“腫瘤戰(zhàn)場(chǎng)"本身,擁有著一套截然不同的代謝規(guī)則?
今天,我們把目光從肝臟移開,聚焦于那個(gè)決定前藥最終命運(yùn)的局部環(huán)境:腫瘤細(xì)胞微粒體。
01 經(jīng)典模型的“陷阱":為何肝微粒體數(shù)據(jù)會(huì)“說謊"?
在藥物研發(fā)的早期,使用肝微粒體評(píng)估前藥的活化效率,是成本低廉、通量高的標(biāo)準(zhǔn)操作(詳見文章鏈接:經(jīng)典微粒體系列(一)——大鼠肝微粒體)。然而,這個(gè)模型的數(shù)據(jù),有時(shí)恰恰是巨大的陷阱,可以直觀地表現(xiàn)為下圖所示的“數(shù)據(jù)鴻溝":

(圖1: 數(shù)據(jù)鴻溝 來源:齊氏生物)
肝微粒體模型的預(yù)設(shè)前提是:
1. 活化主場(chǎng)在肝臟:藥物進(jìn)入體循環(huán)后,主要(或首先)在肝臟被代謝激活。
2. 酶環(huán)境高度濃縮:微粒體富含高活性的CYP450等I相代謝酶,能快速給出“是/否"可被活化的明確信號(hào)。
3. 體系純凈無干擾:排除了細(xì)胞攝取、外排、胞內(nèi)分布、非靶標(biāo)代謝等復(fù)雜因素。
然而,對(duì)于許多靶向腫瘤的前藥,尤其是那些設(shè)計(jì)為在腫瘤局部被特異性激活的“靶向前藥",這個(gè)前提本身就是錯(cuò)的。它的戰(zhàn)場(chǎng),從來就不在肝臟。
02 腫瘤細(xì)胞 vs 肝細(xì)胞:兩個(gè)世界的代謝軍備競(jìng)賽
當(dāng)藥物離開肝臟的“標(biāo)準(zhǔn)測(cè)試場(chǎng)",進(jìn)入腫瘤細(xì)胞的“真實(shí)戰(zhàn)場(chǎng)",它將面對(duì)一套不同的代謝“軍備庫"和“游戲規(guī)則"。
我們可以通過下圖,直觀理解這兩種微粒體模型的本質(zhì)差異,以及為何數(shù)據(jù)會(huì)“脫節(jié)":

(圖2: 肝微粒體VS腫瘤細(xì)胞微粒體 來源:齊氏生物)
如上圖所示,兩者在代謝“軍備庫"和“戰(zhàn)場(chǎng)環(huán)境"上存在根本性不同:
差異一:代謝“軍備庫"不同
肝微粒體是CYP450酶的“重火力集群"。而絕大多數(shù)實(shí)體腫瘤細(xì)胞的微粒體中,經(jīng)典的CYP450酶(如CYP3A4)表達(dá)水平極低甚至缺失。你的前藥那把需要CYP450這把“特定鑰匙"才能打開的鎖,在腫瘤細(xì)胞里面根本找不到匹配的鑰匙。
腫瘤細(xì)胞可能依賴一套不同的、異質(zhì)性的活化酶系統(tǒng),例如:
· 醛酮還原酶(AKR1C3):在某些肉瘤和前列腺癌中高表達(dá)。
· 羧酸酯酶(CES):在肝癌、胃腸道癌中常見。
· 醌氧化還原酶(NQO1):在非小細(xì)胞肺癌等多種實(shí)體瘤中過度表達(dá)。
如果你的前藥不是為這些“腫瘤特異性鑰匙"設(shè)計(jì)的,活化效率自然會(huì)大打折扣。
差異二:細(xì)胞“微環(huán)境"復(fù)雜莫測(cè)
微粒體實(shí)驗(yàn)是生化水平的直接反應(yīng)。而在細(xì)胞內(nèi),前藥需要闖過多重關(guān)卡才能與靶點(diǎn)微粒體相遇:
1. 攝取關(guān):能否有效進(jìn)入細(xì)胞?(跨膜轉(zhuǎn)運(yùn)蛋白?被動(dòng)擴(kuò)散?)
2. 存活關(guān):進(jìn)入后是否被溶酶體降解、或被胞質(zhì)中其他酶非特異性代謝?
3. 定位關(guān):能否順利到達(dá)內(nèi)質(zhì)網(wǎng)(微粒體來源)附近?
4. 競(jìng)爭(zhēng)關(guān):腫瘤細(xì)胞中往往同時(shí)高表達(dá)II相結(jié)合酶(如谷胱甘肽-S-轉(zhuǎn)移酶GST),它們可能迅速將活化的中間體“解毒",使其失活。
03 從“脫節(jié)"到“鏈接":研究策略的轉(zhuǎn)移
要跨越從“體外數(shù)據(jù)"到“細(xì)胞藥效"的鴻溝,需要一套全新的研究策略,如下圖所示:
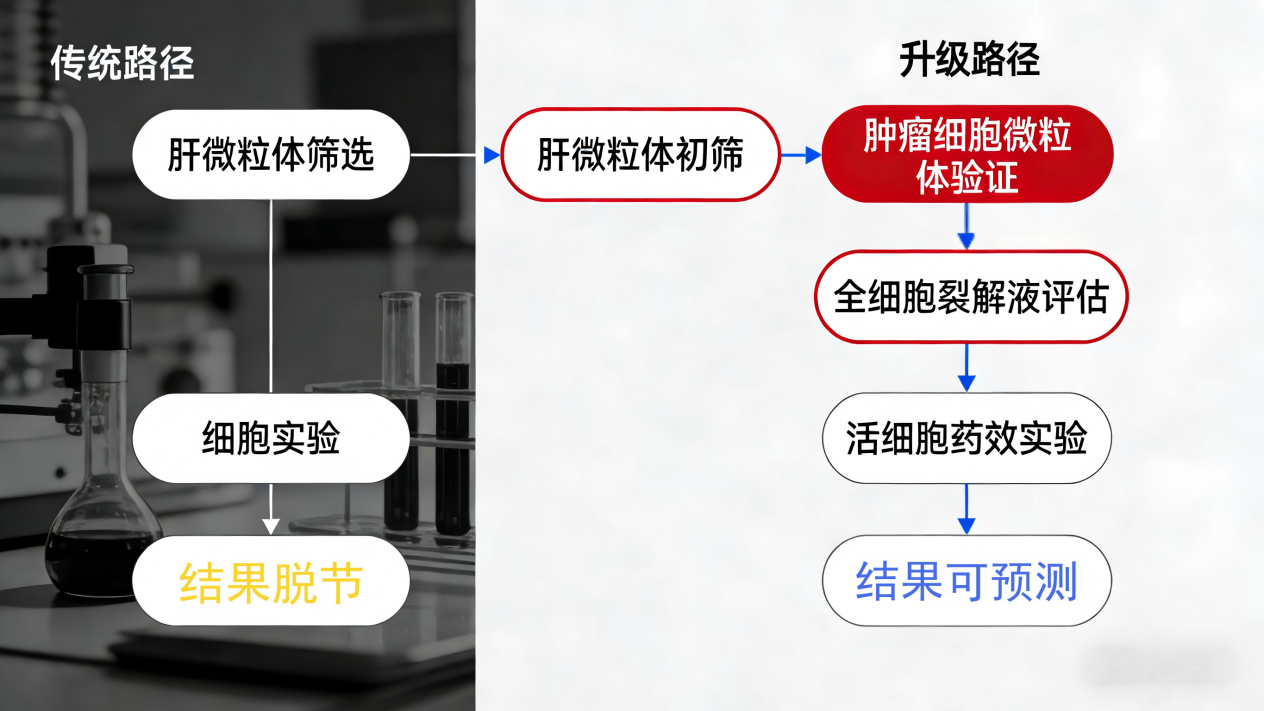
(圖3: 傳統(tǒng)路徑和升級(jí)路徑對(duì)比圖 來源:齊氏生物)
策略一:靶向腫瘤代謝表型進(jìn)行前藥設(shè)計(jì)
在分子設(shè)計(jì)之初,不應(yīng)只考慮“能否被肝酶活化",而應(yīng)深入研究目標(biāo)腫瘤的特異性代謝酶譜,以前藥響應(yīng)那些在腫瘤中高表達(dá)、而在正常組織中低表達(dá)的酶。
策略二:構(gòu)建更貼近真實(shí)的評(píng)價(jià)體系
在肝微粒體數(shù)據(jù)初篩后,必須引入基于腫瘤細(xì)胞的評(píng)價(jià)層級(jí):
1. 腫瘤細(xì)胞微粒體:直接評(píng)估前藥在目標(biāo)腫瘤酶環(huán)境下的活化效率。
2. 全細(xì)胞裂解液:評(píng)估在包含胞質(zhì)/核酶系的更完整體系中的代謝情況。
3. 活細(xì)胞藥效實(shí)驗(yàn):最終驗(yàn)證,并同步監(jiān)測(cè)藥物攝取、代謝物生成等。
策略三:系統(tǒng)表征,避免盲人摸象
對(duì)關(guān)鍵的腫瘤細(xì)胞模型,應(yīng)系統(tǒng)表征其:
· 目標(biāo)活化酶的 mRNA和蛋白表達(dá)水平。
· 競(jìng)爭(zhēng)性/解毒酶的表達(dá)譜。
· 藥物轉(zhuǎn)運(yùn)蛋白(攝取與外排)的表達(dá)情況。
這為解釋實(shí)驗(yàn)數(shù)據(jù)提供了堅(jiān)實(shí)的生物學(xué)背景。
04 結(jié)語:在正確的戰(zhàn)場(chǎng),檢驗(yàn)鋒芒
那位研發(fā)總監(jiān)的困惑,是一個(gè)標(biāo)志性的信號(hào)。它提醒我們,創(chuàng)新藥的研發(fā),尤其是前藥和靶向治療,正日益從“泛代謝"研究走向“精準(zhǔn)局部代謝"研究。肝臟是身體的“代謝中心",但腫瘤是擁有獨(dú)立代謝生態(tài)的“叛亂堡壘"。用衡量中心軍的標(biāo)準(zhǔn)去預(yù)測(cè)叛亂者的行為,自然會(huì)得到令人失望的結(jié)果。
未來,對(duì)于旨在腫瘤局部起效的藥物,其代謝研究的“金標(biāo)準(zhǔn)",或許將不再僅是肝微粒體,而必須包含來自目標(biāo)腫瘤細(xì)胞的微粒體數(shù)據(jù)。 只有在我們計(jì)劃發(fā)動(dòng)攻擊的“戰(zhàn)場(chǎng)"上,檢驗(yàn)鋒芒,才能確保它在真正的戰(zhàn)斗中,一擊制勝!
(代謝π析,剖析無限。本文由[齊氏生物]提供技術(shù)支持。我們不僅提供高質(zhì)量的肝微粒體,更致力于開發(fā)涵蓋多種腫瘤細(xì)胞系的微粒體產(chǎn)品與研究方案,幫助您在新藥研發(fā)的早期,就在正確的戰(zhàn)場(chǎng)上驗(yàn)證代謝策略,讓數(shù)據(jù)真正指向成功。)


 關(guān)注公眾號(hào)
關(guān)注公眾號(hào)  移動(dòng)端瀏覽
移動(dòng)端瀏覽